1 Introdução
A decomposição do movimento vibratório em componentes dinamicamente independentes é chamada de decomposição de modo normal.
O “complicado” é resultado da superposição de “descomplicados.”
A vibração molecular é resultado da superposição de modos normais, ou, se quiser, sobreposição de vibrações nítidas, independentes e desacopladas.
O modo normal é a maneira mais organizada de movimento vibracional. Vamos exemplificar com a molécula de água. A estar a água em um modo normal específico, cada átomo (hidrogênio, hidrogênio e oxigênio) atinge seu deslocamento máximo ao mesmo tempo e passa por sua posição de equilíbrio ao mesmo tempo. Isso quer dizer que vibram com a mesma frequência \((\nu)\). Considere rotular os átomos por \(1,2,3\). Em um modo normal:
\[\begin{equation} \nu ^{(1)} = \nu ^{(2)} = \nu ^{(3)} . \tag{1.1} \end{equation}\]
Porém, a situação (1.1) não significa que os átomos vão sempre vibrar com a mesma amplitude \((A)\). A amplitude pode alterar.
A Fig. 1.1 foi construída para exclarecer a igualdade de frequência e a possível desigualdade de amplitude.
Uma molécula diatômica, na representação de massa reduzida, vibra no modo normal de frequência \(\nu\).
No caso (a), a amplitude de vibração é \(A_a\). No (b), \(A_b\). E no (c), \(A_c\).
No tempo \(t_{I}\), atinge-se a amplitude máxima. No \(t_{II}\), passa-se pela posição de equilíbrio. E no \(t_{III}\), atinge-se novamente a amplitude máxima.
Pela construção da figura:
\[\begin{equation} \begin{aligned} A _ b &= 2 A _ a ,\\ A _ c &= 3 A _ a . \end{aligned} \tag{1.2} \end{equation}\]
Se as frequências nos três casos são iguais, então, os períodos nos três casos também são iguais. De fato, o período para se realizar uma oscilação completa é sempre \(\mathtt{T} = 1/\nu\). Portanto, as velocidades das oscilações são diferentes. A utilizar os deslocamentos de 1 ciclo, pode-se estimar a velocidade média em cada caso:
\[\begin{equation} \begin{aligned} v _ a &= \frac{4A _ a}{T}, \\ v _ b &= \frac{4A _ b}{T} = 2v _ a, \\ v _ c &= \frac{4A _ c}{T} = 3v _ a. \end{aligned} \tag{1.3} \end{equation}\]
Há relação: o caso de maior amplitude – (c) – é o caso de maior velocidade \((3v _ a)\), e o caso de menor amplitude – (a) – é o caso de menor velocidade \((v _ a)\). Em outras palavras, o caso de maior amplitude é o de maior energia, e o caso de menor amplitude é o de menor energia. Podemos resumir assim:
Em um modo de frequência única, o caso de maior energia é o de maior amplitude de vibração.
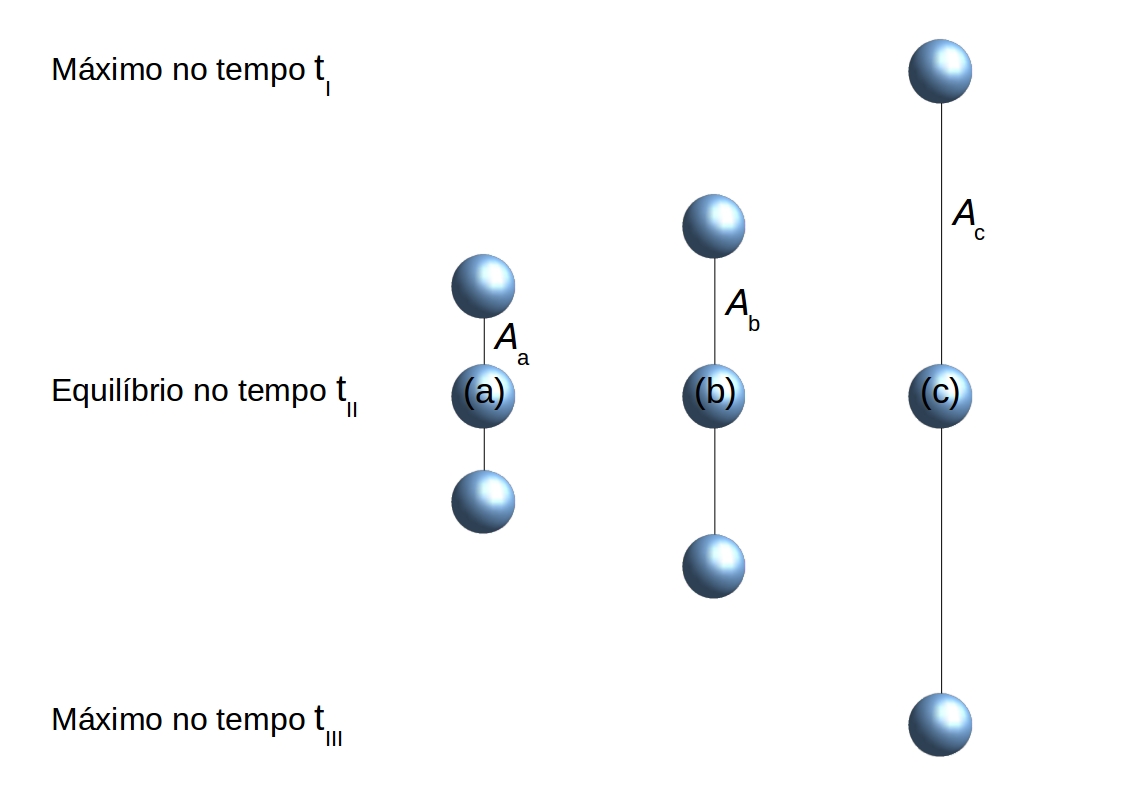
Figura 1.1: Molécula diatômica na representação de massa reduzida. Nas situações (a), (b) e (c), a molécula vibra com a mesma frequência, porém, com amplitudes diferentes.
A energia vibracional, do ponto de vista da mecânica quântica, é discutida no artigo: Energia Vibracional e Rotacional de Molécula Diatômica. No modelo harmônico, a energia vibracional é:
\[\begin{equation} G _ {\nu} = \left( \nu + \tfrac{1}{2} \right) \overline{\nu} . \tag{1.4} \end{equation}\]
Nessa fórmula, \(\nu\) é o número quântico vibracional \((0,1,2,3...)\); e \(\overline{\nu}\) é a frequência de vibração em unidade \(\rm {cm}^{-1}\) (número de onda).
Uma molécula, no estado fundamental do modo \(\overline{\nu}_{\star}\), vibra com a energia \(G _ 0 = \tfrac{1}{2} \overline{\nu}_{\star}\).
A mesma molécula, no primeiro estado excitado do mesmo modo, vibra com a \(G _ 1 = \tfrac{3}{2} \overline{\nu}_{\star}\).
A mesma molécula, agora no segundo estado excitado do mesmo modo, vibra com a \(G _ 2 = \tfrac{5}{2} \overline{\nu}_{\star}\).
E assim por diante.
A lembrar que, em um modo normal, o caso de maior energia é o caso de maior amplitude, conclui-se que a molécula no estado fundamental possui a menor amplitude de vibração, e a amplitude aumenta com o aumento do número quântico.
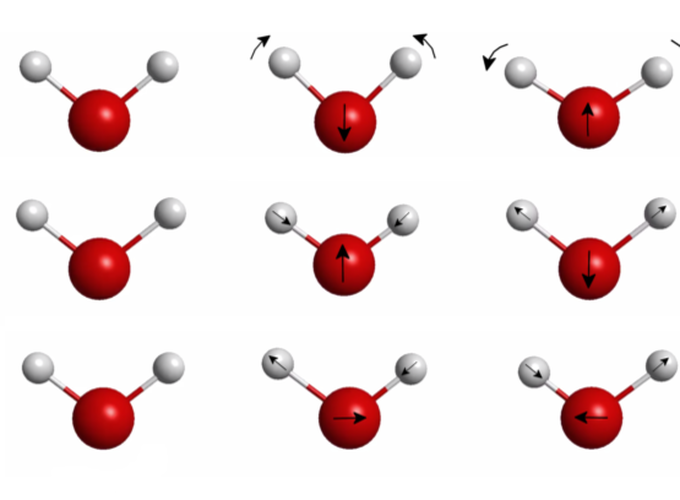
2 Modos normais de vibração da água
Uma molécula tridimensional formada por \(N\) átomos possui \(M\) modos normais de vibração:
\[\begin{equation} M = 3N - 6. \tag{2.1} \end{equation}\]
Segundo a equação (2.1), a molécula de água \((N=3)\) possui 3 modos normais de vibração. Neste trabalho, as frequências dos modos foram determinadas por meio de cálculo ab initio, utilizando o software GAMESS [ver link do portal nas referências]:
\[\begin{equation} \begin{aligned} \overline{\nu} _ {\rm 1} &= 1580\ {\rm cm^{-1}}, \\ \overline{\nu} _ {\rm 2} &= 3602\ {\rm cm^{-1}}, \\ \overline{\nu} _ {\rm 3} &= 3826\ {\rm cm^{-1}}. \end{aligned} \tag{2.2} \end{equation}\]
A Fig. 2.1 apresenta os modos normais de vibração da água. Replicando a equação (1.4), a energia de cada modo é:
\[\begin{equation} \begin{aligned} G _ {\nu _ 1} = \left(\nu _ {1} + \tfrac{1}{2} \right) \overline{\nu} _ {1} ,\\ G _ {\nu _ 2} = \left(\nu _ {2} + \tfrac{1}{2} \right) \overline{\nu} _ {2} ,\\ G _ {\nu _ 3} = \left(\nu _ {3} + \tfrac{1}{2} \right) \overline{\nu} _ {3} . \end{aligned} \tag{2.3} \end{equation}\]
Os primeiros valores das energias (2.3) são listados na Tabela 2.1.
| Frequência de modo normal \((\rm {cm}^{-1})\) | Número quântico | Energia \((\rm {cm}^{-1})\) |
|---|---|---|
| \(\overline{\nu}_{1} = 1580\) | \(\nu_{1}=0\) | \(G_0=790\) |
| \(\nu_{1}=1\) | \(G_1=2370\) | |
| \(\nu_{1}=2\) | \(G_2=3950\) | |
| \(\nu_{1}=3\) | \(G_3=5530\) | |
| \(---\) | \(-----\) | |
| \(\overline{\nu}_{2} = 3602\) | \(\nu_{2}=0\) | \(G_0=1801\) |
| \(\nu_{2}=1\) | \(G_1=5403\) | |
| \(\nu_{2}=2\) | \(G_2=9005\) | |
| \(\nu_{2}=3\) | \(G_3=12607\) | |
| \(---\) | \(-----\) | |
| \(\overline{\nu}_{3} = 3826\) | \(\nu_{3}=0\) | \(G_0=1913\) |
| \(\nu_{3}=1\) | \(G_1=5739\) | |
| \(\nu_{3}=2\) | \(G_2=9565\) | |
| \(\nu_{3}=3\) | \(G_3=13391\) |
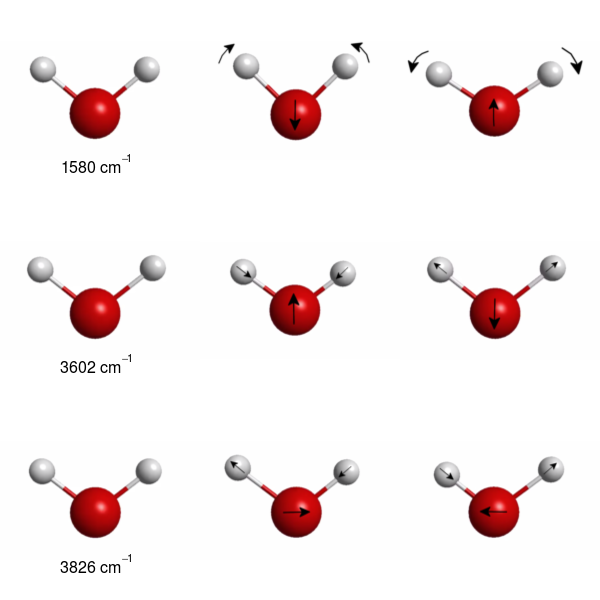
Figura 2.1: Três modos normais de vibração da água.
3 Modos combinados de vibração da água
Além da vibração normal, a molécula de água também pode ser encontrada em uma vibração combinada, oscilando de acordo com uma superposição de modos normais. Na vibração combinada, a energia da molécula é igual à soma das energias dos modos normais:
\[\begin{equation} W _ {(\nu _ 1, \nu _ 2, \nu _ 3)} = \left(\nu _ {1} + \tfrac{1}{2} \right) \overline{\nu} _ {1} + \left(\nu _ {2} + \tfrac{1}{2} \right) \overline{\nu} _ {2} + \left(\nu _ {3} + \tfrac{1}{2} \right) \overline{\nu} _ {3} . \tag{3.1} \end{equation}\]
As frequências normais de vibração da água foram impressas no local (2.2).
Combinando os números quânticos \((\nu_1,\nu_2,\nu_3)\), pode-se ordenar as energias vibracionais da água. Por exemplo, a menor energia ocorre para \((\nu_1,\nu_2,\nu_3) = (0,0,0)\), e tem o valor \(W_{(0,0,0)} = 4504\ {\rm cm^{-1}}\); a Tabela 3.1 apresenta outros valores.
| Modo | Números quânticos | Energia \(({\rm cm^{-1}})\) |
|---|---|---|
| Combinado | \((0,0,0)\) | \(W_{(0,0,0)}=4504\) |
| Combinado | \((1,0,0)\) | \(W_{(1,0,0)}=6084\) |
| Combinado | \((2,0,0)\) | \(W_{(2,0,0)}=7664\) |
| Combinado | \((0,1,0)\) | \(W_{(0,1,0)}=8106\) |
| Combinado | \((0,0,1)\) | \(W_{(0,0,1)}=8330\) |
| Combinado | \((3,0,0)\) | \(W_{(3,0,0)}=9244\) |
| Combinado | \((1,1,0)\) | \(W_{(1,1,0)}=9686\) |
| Combinado | \((1,0,1)\) | \(W_{(1,0,1)}=9910\) |
| Combinado | \((2,1,0)\) | \(W_{(2,1,0)}=11266\) |
| Combinado | \((2,0,1)\) | \(W_{(2,0,1)}=11490\) |
| Combinado | \((0,2,0)\) | \(W_{(0,2,0)}=11708\) |
| Combinado | \((0,1,1)\) | \(W_{(0,1,1)}=11932\) |
| Combinado | \((0,0,2)\) | \(W_{(0,0,2)}=12156\) |
| Combinado | \((3,1,0)\) | \(W_{(3,1,0)}=12846\) |
| Combinado | \((3,0,1)\) | \(W_{(3,0,1)}=13070\) |
| Combinado | \((1,2,0)\) | \(W_{(1,2,0)}=13288\) |
| Combinado | \((1,1,1)\) | \(W_{(1,1,1)}=13512\) |
4 Conclusão
A vibração da água pode ocorrer em modo normal, organizado, no qual os átomos passam pela posição de equilíbrio ao mesmo tempo e vibram na mesma frequência. De acordo com a igualdade de frequência e desigualdade de amplitude, a molécula em modo de frequência única pode modificar sua energia (amplitude) sem alterar sua frequência vibracional. A vibração da água também pode ocorrer em modo combinado, no qual frequências são sobrepostas de acordo com superposição de modos normais.
Referências
Portal GAMESS: General Atomic and Molecular Electronic Structure System.
Link para Recent Developments in GAMESS.